| Trichomonas vaginalis | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
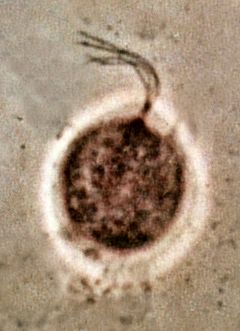 T. vaginalis vista con microscopio de contraste de fase | |||||||||||||||
| Clasificación científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| Trichomonas vaginalis (Donné 1836) | |||||||||||||||
Trichomonas vaginalis é uha especie de protozoo flaxelado anaeróbico, que pode orixinar unha infección denominada tricomoníase, que é a infección protozoaria humana máis común nos países industrializados.[1] Só afecta aos seres humanos. Estímase que as taxas de infección en homes e mulleres son as mesmas, aínda que nas mulleres é sintomática, mentres que nos homes é xeralmente asintomática e pasa desapercibida. A transmisión ten lugar normalmente de forma directa porque a forma de trofozoíto do protozoo non orixina quistes, polo que é unha enfermidade de transmisión sexual. A OMS estima que hai 160 millóns de casos desta infección no mundo ao ano.[2][3]
Características xerais
[editar | editar a fonte]- Só ten un hóspede (parasito monoxeno), é cosmopolita e ten unha única forma celular no seu ciclo vital, o trofozoíto, xa que non forma quistes.
- O trofozoíto de T. vaginalis é oval e flaxelado, ou ten forma de pera en preparacións microscópicas húmidas. É un pouco meirande que un leucocito do sangue, e mide 9 x 7 μm como media. Preto do seu citostoma saen cinco flaxelos; catro deles son anteriores e libres e esténdense xuntos fóra da célula, e o quinto dóbrase cara a atrás ao longo da superficie do microorganismo formando unha especie de membrana ondulante. Paralelo a dita membrana discorre polo interior da célula un feixe de microtúbulos denominado costa. A función do quinto flaxelo non se coñece.[4]
- Posúe un aparato de Golgi asociado a microfilamentos (os filamentos parabasais) que, en conxunto, forman o denominado corpo parabasal.
- Atravesando o citoplasma como un eixe e sobresaíndo polo extremo posterior e en dirección oposta ao conxunto de catro flaxelos, presenta unha estrutura formada por microtúbulos denominada axostilo. Este axostilo, na súa parte anterior, faise máis amplo e cobre parcialmente o núcleo. O axostilo pode utilizarse para adherirse a superficies e pode tamén causar danos no tecido nas tricomoníases.[4] Como continuación do axostilo cara á parte anterior hai outra estrutura de microtúbulos, a pelta, que cobre parcialmente as estruturas basais dos flaxelos.
- O núcleo, que posúe un endosoma, está disposto na zona anterior, preto do punto de inserción dos flaxelos. Nas tinguiduras, o conxunto núcleo-corpo parabasal-axostilo (parte anterior)-pelta adoita tinguirse como unha masa única.
- Carece de mitocondrias e posúe no seu lugar uns orgánulos chamados hidroxenosomas situados en posición paracostal (preto da costa) e paraxostilar (preto do axostilo), que producen enerxía en condicións anaeróbicas.
- O trofozoito é a forma vexetativa que se alimenta, reproduce e infecta.
- Alimentación por fagocitose e pinocitose de bacterias, descamacións celulares e leucocitos (pode producir leucopenia).
- Reprodución por división binaria lonxitudinal, podendo formar poboacións de millóns de individuos en pouco tempo. Non presenta reprodución sexual.
Ciclo vital e infección
[editar | editar a fonte]T. vaginalis vive exclusivamente no tracto uroxenital dos seres humanos. Nas mulleres pode encontrarse na vaxina e na uretra, mentres que nos homes pode atoparse na uretra, a próstata e o epidídimo. Non se pode encontrar en ningún outro órgano ou medio, a excepción de en cultivos de laboratorio, xa que sobrevive poucas horas fóra do corpo. T. vaginalis necesita para o seu desenvolvemento óptimo un pH de 5,5, polo que non vai poder sobrevivir nunha vaxina sa, cuxo pH é máis ácido, de 4-4,5). Porén, unha vez que prospera a infección o propio parasito causará un aumento da alcalinidade do medio para favorecer o seu crecemento. Desde ese momento, os trofozoitos dividiranse incrementando o seu número. No momento en que se produza un contacto sexual os trofozoitos estarán en disposición de infectar ao novo hospedador.
Funcións das proteínas
[editar | editar a fonte]T. vaginalis é un dos poucos eucariotas que carece de mitocondrias e, por tanto, dos encimas e citocromos necesarios para realizar a fosforilación oxidativa. Obtén os nutrientes do exterior transportándoos a través da membrana plasmática ou por fagocitose. O organismo pode obter a enerxía que precisa usando unha pequena cantidade de encimas pola vía da glicólise da glicosa a glicerol e succinato no seu citoplasma, seguido dunha conversión posterior do piruvato e malato a hidróxeno e acetato nun orgánulo especial chamado hidroxenosoma.[5]
Factores de virulencia
[editar | editar a fonte]Unha das características distintivas de T. vaginalis son os factores de adherencia que ten, que lle permiten a colonización do epitelio cervicovaxinal das mulleres. A adherencia que mostra este organismo é específica para as células do epitelio vaxinal e depende do pH, tempo e temperatura. Este proceso está mediado por varios factores de virulencia, algúns dos cales son microtúbulos e microfilamentos, encimas adhesinas, e cisteína proteinases. As adhesinas son catro encimas de tricomónadas chamados AP65, AP51, AP33, e AP23, que median a interacción do parasito con moléculas receptoras das células do epitelio vaxinal.[6] As cisteína proteinases poden ser outro factor de virulencia porque estas proteínas de 30 kD non só se unen á superficie das células do hóspede senón que tamén poden degradar as proteínas da matriz extracelular como a hemoglobina, fibronectina ou coláxeno IV.[7]
Xenoma
[editar | editar a fonte]O xenoma de T. vaginalis ten un tamaño dunhas 160 megabases,[8] polo que é dez veces máis grande que o predito polas primeiras medicións de tamaño de cromosomas en xel [9] (O xenoma humano é de ~3,5 xigabases en compoaración).[10] Ata 2/3 das secuencias xenómicas de T. vaginalis son repetitivas e elementos transpoñibles, o que indica que houbo unha expansión masiva do xenoma evolutivamente recente. O número toral de xenes codificantes de proteínas preditos é de ~98.000, o cal inclúe ~38.000 xenes "repetidos" (xenes de tipo vírico, de tipo transposón, de tipo retrotransposón, e repeticións non clasificadas, todas cun alto número de copias e un baixo polimorfismo). Aproximadamente 26.000 destes xenes codificadores de proteínas foron clasificados como "apoiados nas evidencias" (o que quere dicir que son xenes de proteínas coñecidas ou a que son ESTs), e do resto dos xenes non se coñece a súa función. Estas extraordinarias estatísticas do seu xenoma probablemente cambiarán a cifras máis pequenas a medida que a secuencia xenómica, que actualemnte está moi fragmentada debido á dificultade de ordenar o ADN repetitivo, sexa ensamblada en cromosomas, e a medida que se teñan máis datos de transcrición (ESTs, micromatrices de ADN). Pero, malia todo, parece que o número de xenes deste parasito está como mínimo á par co do seu hóspede humano.
En 2007 comezou a funcionar TrichDB.org, que é un repositorio de datos xenómicos público de libre acceso e un servizo de recuperación de datos dedicado aos datos das tricomónadas a escala xenómica. O sitio web contén actualmente todos os datos de proxectos de secuenciación de T. vaginalis, varias librarías de EST, e ferramentas para a mostra e minado de datos. TrichDB é parte do proxecto de bases de datos xenómicas funcionais do NIH/NIAID EupathDB.[11]
Evolución
[editar | editar a fonte]A bioloxía de T. vaginalis ten implicacións no coñecemento da orixe da reprodución sexual en eucariotas. En T. vaginalis nunca se observou meiose, que é unha fase fundamental no ciclo sexual dos eucariotas. Porén, cando Malik et al.[12] estudaron a presenza en T. vaginalis de 29 xenes que se sabe que exercen a súa función na meiose, atoparon que 27 deles estaban presentes, incluíndo 8 dos 9 xenes que son específicos da meiose en organismos modelo. Estes descubrimentos suxiren que a capacidade para facer a meiose, e, por tanto, a reprodución sexual, estaba presente nos antepasados recentes de T. vaginalis. Un total de 21 xenes dos 27 da meiose atópanse tamén noutro parasito, o Giardia lamblia (tamén chamado G. intestinalis), o que indica que estes xenes meióticos estaban presentes nun antepasado común de T. vaginalis e G. lamblia. Como estas dúas especies son descendentes de liñaxes que son moi diverxentes entre os eucariotas, Malik et al.[12] sinalaron que estes xenes meióticos probablemente xa estaban presentes no antecesor común de todos os eucariotas. Estas consideracións, xunto con datos doutras especies, suxiren que a meiose, e a reprodución sexual, xa estaba presente no antepasado común de todos os eucariotas.[13]
Aspectos clínicos
[editar | editar a fonte]- Artigo principal: Tricomoníase.
Mecanismos de infección
[editar | editar a fonte]Trichomonas vaginalis é o axente causante da tricomoníase, que é unha enfermidade de transmisión sexual que afecta ao tracto uroxenital.[2][14] Máis de 160 millóns de persoas se infectan por este protozoo no mundo cada ano.[2]
Síntomas
[editar | editar a fonte]
A tricomoníase, é unha causa común de vaxinite nas mulleres, pero nos homes esta infección pode ser asintomática ou presentar síntomas de uretrite. É característica nas mulleres unha descarga vaxinal escumosa cun cheiro a mofo.[15]
Signos
[editar | editar a fonte]O 20% das mulleres con esta infección teñen unha vaxina ou cérvix eritematoso con colpitis macularis, e áreas punteadas de exsudación.[16][17][18] Isto débese á dilatación capilar como resultado da resposta inflamatoria.
Complicacións
[editar | editar a fonte]Algunhas complicacións da infección por T. vaginalis nas mulleres son: parto prematuro, baixo peso do neno ao nacer, e aumento da mortalidade e predisposición á infección por VIH, SIDA, e cancro cervical.[19] T. vaginalis tamén se atopou no tracto urinario, trompas de Falopio, e pelve. Os condóns son efectivos para reducir a transmisión, pero non eliminan o risco por completo.[20]
Investigacións recentes suxiren que pode haber unha ligazón entre a infección por T. vaginalis en machos e un subseguinte cancro de próstata agresivo.[21]
Diagnose
[editar | editar a fonte]Clasicamente, faise cun frotis cervical (proba Pap ou Papanicolau), no cal as células das mulleres infectadas teñen un "halo" transparente arredor do núcleo. T. vaginalis era diagnosticada tradicionalmente facendo unha preparación húmida, na cal se observaba unha motilidade en "sacarrollas" do parasito. Actualmente, o método máis común de diagnóstico é o cultivo durante un día,[22][23] cun rango de sensibilidade de 75-95%.[24] Hai métodos novos aínda pouco usados, pero de grande sensibilidade, como a proba de antíxenos rápida e a amplificación mediada por transcrición.[24] Tamén se pode detectar por medio da PCR, usando cebadores específicos para GENBANK/L23861.[25]
Tratamento
[editar | editar a fonte]A infección trátase e cúrase con metronidazol[26] ou tinidazole. O tratamento tamén o deberían aplicar as parellas sexuais das persoas afectadas, xa que poden ser portadores asintomáticos.[15][27]
Aumento da susceptibilidade ao VIH
[editar | editar a fonte]Os danos causados por Trichomonas vaginalis ao epitelio vaxinal aumentan a susceptibilidade das mulleres á infección polo VIH. Ademais da inflamación, o parasito tamén causa a lise das células epiteliais e de eritrocitos na área, o que orixina máis inflamación e altera as barreiras protectoras normais do epitelio. Ter unha infección por T. vaginalis tamén pode incrementar as posibilidades de que unha muller infectada transmita o VIH á súa parella sexual.[28][29]
Notas
[editar | editar a fonte]- ↑ Soper, D (2004). "Trichomoniasis: under control or undercontrolled?". American Journal of Obstetrics and Gynecology 190 (1): 281–90. PMID 14749674. doi:10.1016/j.ajog.2003.08.023.
- ↑ 2,0 2,1 2,2 Harp, Djana F.; Chowdhury, Indrajit (2011). "Trichomoniasis: Evaluation to execution". European Journal of Obstetrics & Gynecology and Reproductive Biology 157 (1): 3–9. PMID 21440359. doi:10.1016/j.ejogrb.2011.02.024.
- ↑ Hook, Edward W. (1999). "Trichomonas vaginalis—No Longer a Minor STD". Sexually Transmitted Diseases 26 (7): 388–9. PMID 10458631. doi:10.1097/00007435-199908000-00004.
- ↑ 4,0 4,1 Ryan, Kenneth James; Ray, C. George; Sherris, John C., eds. (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. ISBN 978-0-8385-8529-0.
- ↑ Upcroft, P.; Upcroft, J. A. (2001). "Drug Targets and Mechanisms of Resistance in the Anaerobic Protozoa". Clinical Microbiology Reviews 14 (1): 150–64. PMC 88967. PMID 11148007. doi:10.1128/CMR.14.1.150-164.2001.
- ↑ Arroyo, R.; Engbring, J.; Alderete, J. F. (1992). "Molecular basis of host epithelial cell recognition by Trichomonas vaginalis". Molecular Microbiology 6 (7): 853–862. PMID 1602965. doi:10.1111/j.1365-2958.1992.tb01536.x.
- ↑ Mendoza-Lopez, M. R.; Becerril-Garcia, C.; Fattel-Facenda, L. V.; Avila-Gonzalez, L.; Ruiz-Tachiquin, M. E.; Ortega-Lopez, J.; Arroyo, R. (2000). "CP30, a Cysteine Proteinase Involved in Trichomonas vaginalis Cytoadherence". Infection and Immunity 68 (9): 4907–12. PMC 101697. PMID 10948104. doi:10.1128/IAI.68.9.4907-4912.2000.
- ↑ Carlton, J. M.; Hirt, R. P.; Silva, J. C.; Delcher, A. L.; Schatz, M.; Zhao, Q.; Wortman, J. R.; Bidwell, S. L.; Alsmark, U. C. M. (2007). "Draft Genome Sequence of the Sexually Transmitted Pathogen Trichomonas vaginalis". Science 315 (5809): 207–12. PMC 2080659. PMID 17218520. doi:10.1126/science.1132894.
- ↑ Lehker, M. W.; Alderete, J. F. (1999). "Resolution of Six Chromosomes of Trichomonas vaginalis and Conservation of Size and Number among Isolates". The Journal of Parasitology 85 (5): 976–9. JSTOR 3285842. PMID 10577741. doi:10.2307/3285842.
- ↑ Zimmer, C. (2007). "EVOLUTION: Jurassic Genome". Science 315 (5817): 1358–9. PMID 17347424. doi:10.1126/science.315.5817.1358.
- ↑ Aurrecoechea, Cristina; Brestelli, John; Brunk, Brian P.; Carlton, Jane M.; Dommer, Jennifer; Fischer, Steve; Gajria, Bindu; Gao, Xin; Gingle, Alan (2009). "GiardiaDB and TrichDB: integrated genomic resources for the eukaryotic protist pathogens Giardia lamblia and Trichomonas vaginalis". Nucleic Acids Research 37 (Database issue): D526–30. PMC 2686445. PMID 18824479. doi:10.1093/nar/gkn631.
- ↑ 12,0 12,1 Malik SB, Pightling AW, Stefaniak LM, Schurko AM, Logsdon JM (2008). "An expanded inventory of conserved meiotic genes provides evidence for sex in Trichomonas vaginalis". PLoS ONE 3 (8): e2879. PMC 2488364. PMID 18663385. doi:10.1371/journal.pone.0002879.
- ↑ Bernstein H, Bernstein C, Michod RE (2012). DNA repair as the primary adaptive function of sex in bacteria and eukaryotes. Chapter 1: pp.1-49 in: DNA Repair: New Research, Sakura Kimura and Sora Shimizu editors. Nova Sci. Publ., Hauppauge, N.Y. ISBN 978-1-62100-808-8 https://www.novapublishers.com/catalog/product_info.php?products_id=31918 Arquivado 29 de outubro de 2013 en Wayback Machine.
- ↑ Johnston VJ, Mabey DC (2008). "Global epidemiology and control of Trichomonas vaginalis". Current Opinion in Infectious Diseases 21 (1): 56–64. PMID 18192787. doi:10.1097/QCO.0b013e3282f3d999.
- ↑ 15,0 15,1 Nanda, N; Michel, RG; Kurdgelashvili, G; Wendel, KA (2006). "Trichomoniasis and its treatment". Expert review of anti-infective therapy 4 (1): 125–35. PMID 16441214. doi:10.1586/14787210.4.1.125.
- ↑ Swygard H, Seña AC, Hobbs MM, Cohen MS (2004). "Trichomoniasis: clinical manifestations, diagnosis and management". Sex Transm Infect 80 (2): 91–5. PMC 1744792. PMID 15054166. doi:10.1136/sti.2003.005124.
- ↑ Petrin D, Delgaty K, Bhatt R, Garber G (1998). "Clinical and microbiological aspects of Trichomonas vaginalis". Clin. Microbiol. Rev. 11 (2): 300–17. PMC 106834. PMID 9564565.
- ↑ Garber GE (2005). "The laboratory diagnosis of Trichomonas vaginalis". Can J Infect Dis Med Microbiol 16 (1): 35–8. PMC 2095007. PMID 18159526.
- ↑ Schwebke, J. R.; Burgess, D. (2004). "Trichomoniasis". Clinical Microbiology Reviews 17 (4): 794–803, table of contents. PMC 523559. PMID 15489349. doi:10.1128/CMR.17.4.794-803.2004.
- ↑ "Trichomoniasis". CDC Fact Sheet. Centers for Disease Control and Prevention. 2007-12-17. Consultado o 2010-06-11.
- ↑ Stark, Jennifer R.; Judson, Gregory; Alderete, John F.; Mundodi, Vasanthakrishna; Kucknoor, Ashwini S.; Giovannucci, Edward L.; Platz, Elizabeth A.; Sutcliffe, Siobhan; Fall, Katja (2009). "Prospective Study of Trichomonas vaginalis Infection and Prostate Cancer Incidence and Mortality: Physicians' Health Study". JNCI Journal of the National Cancer Institute 101 (20): 1406–11. PMC 2765259. PMID 19741211. doi:10.1093/jnci/djp306.
- ↑ Ohlemeyer, C; Hornberger, L; Lynch, D; Swierkosz, E (1998). "Diagnosis of Trichomonas vaginalis in adolescent females: InPouch TV® culture versus wet-mount microscopy". Journal of Adolescent Health 22 (3): 205–8. PMID 9502007. doi:10.1016/S1054-139X(97)00214-0.
- ↑ Sood, Seema; Mohanty, Srujana; Kapil, Arti; Tolosa, Jorge; Mittal, Suneeta (2007). "InPouch TV culture for detection of Trichomonas vaginalis" (PDF). The Indian journal of medical research 125 (4): 567–71. PMID 17598943. Arquivado dende o orixinal (PDF) o 04 de novembro de 2013. Consultado o 03 de novembro de 2013.
- ↑ 24,0 24,1 Huppert, Jill S.; Mortensen, Joel E.; Reed, Jennifer L.; Kahn, Jessica A.; Rich, Kimberly D.; Miller, William C.; Hobbs, Marcia M. (2007). "Rapid Antigen Testing Compares Favorably with Transcription‐Mediated Amplification Assay for the Detection of Trichomonas vaginalis in Young Women". Clinical Infectious Diseases 45 (2): 194–8. PMID 17578778. doi:10.1086/518851.
- ↑ Schirm, Jurjen; Bos, Petra A.J.; Roozeboom-Roelfsema, Irene K.; Luijt, Dirk S.; Möller, Lieke V. (2007). "Trichomonas vaginalis detection using real-time TaqMan PCR". Journal of Microbiological Methods 68 (2): 243–7. PMID 17005275. doi:10.1016/j.mimet.2006.08.002.
"Trichomonas vaginalis repeated DNA target for PCR identification". GenBank Nucleotide Database. National Center for Biotechnology Information. L23861.1.
Kengne P, Veas F, Vidal N, Rey JL, Cuny G (1994). "Trichomonas vaginalis: repeated DNA target for highly sensitive and specific polymerase chain reaction diagnosis". Cell. Mol. Biol. (Noisy-le-grand) 40 (6): 819–31. PMID 7812190. - ↑ "Metronidazole". HealthExpress. Consultado o 31 July 2013.
- ↑ Cudmore, S. L.; Delgaty, K. L.; Hayward-Mcclelland, S. F.; Petrin, D. P.; Garber, G. E. (2004). "Treatment of Infections Caused by Metronidazole-Resistant Trichomonas vaginalis". Clinical Microbiology Reviews 17 (4): 783–93, table of contents. PMC 523556. PMID 15489348. doi:10.1128/CMR.17.4.783-793.2004.
- ↑ Mulla, Summaiyaa; Kosambiya, JK; Desai, Vikask; Shethwala, Nimishad (2009). "Sexually transmitted infections and reproductive tract infections in female sex workers". Indian Journal of Pathology and Microbiology 52 (2): 198–9. PMID 19332911. doi:10.4103/0377-4929.48916.
- ↑ Mavedzenge, Sue Napierala; Van der Pol, Barbara; Cheng, Helen; Montgomery, Elizabeth T.; Blanchard, Kelly; de Bruyn, Guy; Ramjee, Gita; Van der Straten, Ariane (2010). "Epidemiological Synergy of Trichomonas vaginalis and HIV in Zimbabwean and South African Women". Sexually Transmitted Diseases 37 (7): 460–6. PMID 20562586. doi:10.1097/OLQ.0b013e3181cfcc4b.
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Markell, E.K., Voge, M., e John D.T. 1990.-Parasitología médica. Interamericana. McGraw-Hill. Madrid.
Ligazóns externas
[editar | editar a fonte]- TIGR's Trichomonas vaginalis genome sequencing project.
- TrichDB: the Trichomonas vaginalis genome sequencing project
- Sitio web do NIH sobre a tricomoníase.
- Taxonomy
- eMedicine article on trichomoniasis.
- Encyclopaedia of life T. vaginalis Arquivado 31 de outubro de 2013 en Wayback Machine.
- Patient UK