| |

| |
| Nazivi | |
|---|---|
| IUPAC naziv
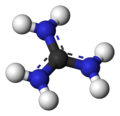
Guanidine
| |
| Identifikacija | |
3D model (Jmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.003.656 |
| UNII | |
| |
| Svojstva | |
| CH5N3 | |
| Molarna masa | 59,07 g/mol |
| Tačka topljenja | 50 °C |
| Kiselost (pKa) | 13.6 (gvanidinijum katjon)[3] |
| Srodna jedinjenja | |
Srodna jedinjenja
|
Gvanidinijum hlorid Nitrogvanidin |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Gvanidin jekristalno jedinjenje jake alkalnosti formirano oksidacijom gvanina. Ovo jedinjenje se koristi u proizvodnji plastike i eksploziva. On je sastojak urina, kao normalni proizvod proteinskog metabolizma. Molekul je bio privi put sintetisan 1861, oksidativnom degradacijom jednog aromatičnog prirodnog proizvoda, guanina, izolovanog iz peruvijskog gvana.[4] Uprkos jednostavnosti molekula, kristalna struktura je opisana tek 148 godina kasnije.[5]