| |
| |
| Nazivi | |
|---|---|
| IUPAC naziv
Arsenitna kiselina
| |
| Drugi nazivi
Arsenitna kiselina
| |
| Identifikacija | |
3D model (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| |
| Svojstva | |
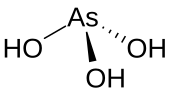
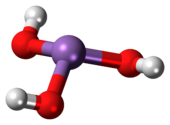
| H3AsO3 | |
| Molarna masa | 125,94 g/mol |
| Agregatno stanje | Postoji samo u vodenom rastvoru |
| Opasnosti | |
| Opasnost u toku rada | Toksična, korozivna |
| Srodna jedinjenja | |
Srodna jedinjenja
|
Arsenatna kiselina |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Arsenitna kiselina je neorgansko jedinjenje sa formulom H3AsO3. Ona je javlja u vodenim rastvorima. Ona nije bila izdvojena kao čist materijal.[3]