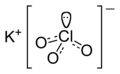
Chloran potasu
|
|

|
| Nazewnictwo
|
|
|
| Nomenklatura systematyczna (IUPAC)
|
| addyt.
|
trioksydochloran(1−) potasu
|
| Inne nazwy i oznaczenia
|
| półsyst.
|
chloran potasu
|
| Stocka
|
chloran(V) potasu
|
| inne
|
daw. chloran potasowy, zwycz. sól Bertholleta, kalichloricum, pot. kalichlorek[1]
|
|
| Ogólne informacje
|
| Wzór sumaryczny
|
KClO
3
|
| Masa molowa
|
122,55 g/mol
|
| Wygląd
|
biały lub prawie biały proszek, granulki lub kryształy[2]
|
| Identyfikacja
|
| Numer CAS
|
3811-04-9
|
| PubChem
|
6426889
|
|
|
| InChI
|
InChI=1S/ClHO3.K/c2-1(3)4;/h(H,2,3,4);/q;+1/p-1
|
| InChIKey
|
VKJKEPKFPUWCAS-UHFFFAOYSA-M
|
|
|
|
| Niebezpieczeństwa
|
| Karta charakterystyki: dane zewnętrzne firmy Sigma-Aldrich [dostęp 2018-07-11]
|
|
|
Globalnie zharmonizowany system
klasyfikacji i oznakowania chemikaliów
|
| Na podstawie Rozporządzenia CLP, zał. VI[5]
|
|
|
|
|
| Zwroty H
|
H271, H302, H332, H411
|
| Zwroty P
|
P210, P220, P221, P261, P370+P378, P371+P380+P375[3]
|
|
|
| NFPA 704
|
Na podstawie
podanego źródła[6]
|
|
|
|
|
| Numer RTECS
|
FO0350000
|
| Dawka śmiertelna
|
LD50 1870 mg/kg (szczur, doustnie)[4]
|
|
| Podobne związki
|
| Inne aniony
|
KClO, KClO
2, KClO
4
|
| Inne kationy
|
NaClO
3, NH
4ClO
3
|
Jeżeli nie podano inaczej, dane dotyczą
stanu standardowego (25 °C, 1000 hPa)
|
|
|
Chloran potasu (nazwa Stocka: chloran(V) potasu), KClO
3 – nieorganiczny związek chemiczny, sól potasowa kwasu chlorowego. Stosowany do produkcji zapałek i materiałów wybuchowych[7].
Otrzymywanie
Na skalę przemysłową otrzymywany jest czasami w procesie elektrolizy roztworu chlorku potasu. W przestrzeni anodowej zachodzą następujące reakcje[8]:
- 2Cl−
→ Cl
2 + 2e−
- Cl
2 + H
2O ⇄ HClO + H+
+ Cl−
- HClO ⇄ H+
+ ClO−
- 2HClO + ClO−
→ ClO−
3 + 2Cl−
+ 2H+
Anody do tego procesu pokrywane są powłokami z RuO
2 lub tytanu, aby zapewnić ich trwałość chemiczną.
W analogicznym procesie elektrochemicznym częściej otrzymuje się chloran sodu (jako roztwór wodny), z którego następnie wytrąca się chloran potasu po dodaniu stałego KCl[8]:
- KCl + NaClO
3 → NaCl + KClO
3↓
Jest to główna przemysłowa metoda produkcji tego związku. Pozostała solanka jest zawracana do elektrolizera i wykorzystywana ponownie[8].
Inną metodą otrzymywania KClO
3 jest przepuszczanie gazowego chloru przez gorący roztwór wodorotlenku potasu[9]:
- 3Cl
2 + 6KOH → KClO
3 + 5KCl + 3H
2O