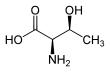
Threonine (afgekort als Thr of T) is een hydrofiel aminozuur. Het is een van de twintig natuurlijk voorkomende α-aminozuren die voor eiwitsynthese wordt gebruikt. De zijketen van threonine bevat een polaire hydroxylgroep, dat interacties aan kan gaan met andere moleculen. In eiwitten speelt threonine een belangrijke rol bij de totstandkoming van de secundaire structuur en bij deelname aan posttranslationele modificatie.
Threonine wordt geclassificeerd als een voor mens en dier essentieel aminozuur, omdat het lichaam de verbinding niet zelf kan aanmaken en enkel uit voeding kan worden verkregen. Micro-organismen zoals E. coli kunnen het aminozuur echter wel zelf vormen, bijvoorbeeld uit asparaginezuur. Threonine wordt gecodeerd door de codons die beginnen met AC (namelijk ACA, ACC, ACG en ACU).
Biochemie
Synthese
In planten en micro-organismen wordt threonine gesynthetiseerd uit asparaginezuur via α-aspartyl-semialdehyde en homoserine.[1] Homoserine ondergaat fosforylering; de ontstane fosfaatester wordt vervolgens gehydrolyseerd waarbij de OH-groep verplaatst wordt. Het threonine dat via deze weg gevormd wordt, vormt de basis van het natuurlijk voorkomende threonine dat de mens en dier nodig heeft. De aanbevolen dagelijkse hoeveelheid voor een volwassene bedraagt ongeveer 20 mg/kg.[2]
Racemisch threonine kan worden bereid uit een alfa-functionalisatiereactie van crotonzuur met behulp van kwik(II)acetaat.[3]
Stofwisseling
Threonine wordt op twee manieren gemetaboliseerd:
- Bij veel dieren wordt threonine omgezet in pyruvaat onder invloed van threoninedehydrogenase. Een tussenproduct in deze route kan thiolyse met CoA ondergaan waarbij acetyl-CoA en glycine ontstaan.
- Bij mensen is het gen dat codeert voor threoninedehydrogenase een inactief pseudogen,[4] dus wordt threonine in het menselijk lichaam omgezet naar 2-ketobutyraat. Het mechanisme van de eerste stap is analoog aan dat van serinedehydratase, en men vermoedt dat de serine- en threoninedehydratasereacties waarschijnlijk gekatalyseerd worden door hetzelfde enzym.[5]
Functies
Threonine is in hoge concentraties aanwezig in het hart, skeletspieren en het centrale zenuwstelsel. Het is nodig om de juiste eiwitbalans in het lichaam te behouden, en helpt bij de vorming van collageen en elastine in de huid.[7] Daarnaast is het betrokken bij de leverfunctie (waaronder bestrijding van leververvetting), lipotrope functies in combinatie met asparaginezuur en methionine en de ondersteuning van het immuunsysteem door de productie van antilichamen en bevordering van thymusactiviteit.[8] Andere voedingsstoffen worden beter geabsorbeerd wanneer threonine aanwezig, en het wordt daarom gebruikt als onderdeel bij de behandeling van geestelijke gezondheid.[9]
Threonine is een voorloper van isoleucine en onbalans kan ontstaan als de synthese vanaf aspartaat onjuiste waarden heeft. Bij mensen kan een tekort aan threonine leiden tot prikkelbaarheid en een algemeen moeilijke persoonlijkheid. Threonine is aanwezig in eiwitrijke producten: vlees, zuivelproducten en eieren, en in kleinere hoeveelheden in tarwekiemen, noten, bonen en groente te vinden.