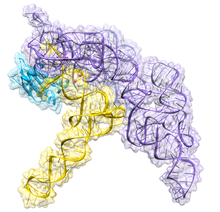
| RNase P bacteriana de clase A | |
|---|---|
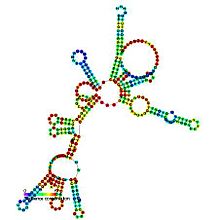 Estrutura secundaria predita e conservación de secuencia da RNaseP_bact_a | |
| Identificadores | |
| Símbolo | RNaseP_bact_a |
| Rfam | RF00010 |
| Outros datos | |
| Tipo de ARN | Xene; ribozima |
| Dominio(s) | Bacterias |
| GO | 0008033 0004526 0030680 |
| Estruturas PDB | PDBe |
| RNase P bacteriana de clase B | |
|---|---|
 Estrutura secundaria predita e conservación de secuencia da RNaseP_bact_b | |
| Identificadores | |
| Símbolo | RNaseP_bact_b |
| Rfam | RF00011 |
| Outros datos | |
| Tipo de ARN | Xene; ribozima |
| Dominio(s) | Bacterias |
| GO | 0008033 0004526 0030680 |
| Estruturas PDB | PDBe |
| RNase P bacteriana | |
|---|---|
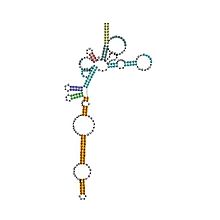 Estrutura secundaria predita e conservación de secuencia da RNase P arqueana | |
| Identificadores | |
| Símbolo | RNaseP_arch |
| Rfam | RF00373 |
| Outros datos | |
| Tipo de ARN | Xene; ribozima |
| Dominio(s) | Arqueas |
| GO | 0008033 0004526 0030680 |
| Estruturas PDB | PDBe |
| RNase arqueana de clase T | |
|---|---|
| Identificadores | |
| Símbolo | RNaseP-T |
| Rfam | RF02357 |
| Outros datos | |
| Tipo de ARN | Xene; ribozima |
| Dominio(s) | Arqueas |
| GO | 0008033 0004526 0030680 |
| Estruturas PDB | PDBe |
A ribonuclease P ou RNase P (EC 3.1.26.5) é un tipo de ribonuclease que corta o ARN. A RNase P é única entre todas as RNases porque non é unha proteína, senón un ribozima (un ARN que actúa como catalizador igual que os enzimas proteicos). A súa función é cortar unha secuencia extra en moléculas precursoras do ARNt.[1] Ademais, a RNase P é un dos dous ribozimas de recambio múltiple que existen na natureza (o outro é o ribosoma), cuxo descubrimento valeulle a Sidney Altman e Thomas Cech a concesión do Premio Nobel de Química de 1989. Na década de 1970, Altman descubriu a existencia dos ARNt precursores que tiñan secuencias nos flancos que non aparecen na molécula madura e foron os primeiros en caracterizar a RNase P e a súa actividade no procesamento da secuencia líder 5' do ARNt precursor. Descubrimentos recentes revelaron tamén que a RNase P ten unha nova función.[2] É necesaria a RNase P nuclear humana para a transcrición normal e eficiente de varios xenes de ARN non codificante pequeno, como os do ARNt, ARNr 5S, ARN da SRP e ARN nuclear pequeno U6 (espliceosomal),[3] que son transcritos pola ARN polimerase III, unha das tres grandes ARN polimerases das células humanas.
En bacterias
[editar | editar a fonte]A RNase P bacteriana ten dous compoñentes: unha cadea de ARN, chamada ARN M1, e unha cadea polipeptídica ou proteína, chamada proteína C5.[4][5] In vivo cómpren ambos os compoñentes para que o ribozima funcione correctamente, pero in vitro o ARN M1 pode actuar el só como catalizador.[1] O papel principal da proteína C5 é mellorar a afinidade de unión ao substrato e a velocidade catalítica do enzima ARN M1 probablemente incrementando a afinidade de unión a un ión metálico no sitio activo. A estrutura cristalina dun holoenzima RNase P bacteriano unido ao ARNt foi resolta recentemente, mostrando como os grandes dominios helicoidais amoreados coaxialmente do ARN da RNase P están implicados no recoñecemento selectivo da forma da diana do pre-ARNt. Esta estrutura cristalina confirma os modelos anteriores de recoñecemento de substrato e catálise, identifica a localización do sitio activo e mostra como os compoñentes da proteína incrementan a funcionalidade da RNase P.[6][7]
RNases P bacterianas das clases A e B
[editar | editar a fonte]A RNase P é unha endorribonuclease moi estendida nos seres vivos, presentre en bacterias, arqueas e eucariotas e tamén en cloroplastos e mitocondrias. A súa actividade mellor caracterizada é a xeración de extremos 5' maduros nos ARNt ao cortar os elementos líder 5' dos ARNt precursores. As RNases P celulares son ribonucleoproteínas (RNP). O ARN das RNAses P bacterianas conserva a súa actividade catalítica en ausencia da subunidade proteica, é dicir, é un ribozima. O ARN da RNase P eucarióticas e arqueanas illadas non conserva a súa función catalítica, pero aínda así é esencial para a actividade catalítica do holoenzima. Aínda que os holoenzimas arqueanos e eucariotas teñen un contido proteico moito maior que os bacterianos, os núcleos de ARN das tres liñaxes son homólogos, e as hélices que corresponden a P1, P2, P3, P4, e P10/11 son comúns a todos os ARN das RNases P celulares. Con todo, hai unha considerable variación na secuencia, especialmente entre os ARN eucariotas.
En arqueas
[editar | editar a fonte]En arqueas as ribonucleoproteínas RNase P constan de 4 ou 5 subunidades proteicas que están asociadas co ARN. Como revelaron experimentos de reconstitución in vitro, estas subunidades proteicas non son individualmente imprescindibles para o procesamento do ARNt que está mediado esencialmente polo compoñente de ARN.[8][9][10] As estruturas das subunidades proteicas da RNase P arqueana resolvéronse por cristalografía de raios X e por RMN, que descubriu novos dominios proteicos e pregamentos fundamentais para o seu funcionamento.
Usando unha xenómica comparada e mellorando os métodos computacionais, atopouse unha forma radicalemnte minimizada do ARN da RNase P, denominada "Tipo T", en todos os xenomas completos na familia filoxenética crenarqueana das Thermoproteaceae, incluíndo especies dos xéneros Pyrobaculum, Caldivirga e Vulcanisaeta.[11] Todas conservan un dominio catalítico convencional, mais carecen dun dominio de especificidade recoñecible. Confirmouse experimentalmente a actividade de procesamento 5′ do ARNt que presenta o ARN por si só. Os ARN da RNase P de Pyrobaculum e Caldivirga son os máis pequenos que se atoparon polo momento na natureza que funcionan como ribozimas que actúan en trans.[11] A perda do dominio de especificidade nestes ARN suxire que a especificidade de substrato está potencialmente alterada.
Argumentouse recentemente que a arquea Nanoarchaeum equitans non posúe RNase P. Os estudos computacionais e experimentais non conseguiron atopar probas da súa existencia. Neste organismo o promotor do ARNt está próximo ao xene do ARNt e pénsase que a transcrición empeza na primeira base do ARNt, o que eliminaría a necesidade de ter unha RNase P.[12]
En eucariotas
[editar | editar a fonte]En eucariotas, como son os humanos e os lévedos, a maioría das RNase P constan dunha cadea de ARN estruturalmente siilar á que se encontra en bacterias [13] xunto con de 9 a 10 proteínas asociadas (a diferenza da única proteína na RNAse bacteriana, a C5).[2][14] Cinco destas subunidades proteicas mostran homoloxía coas correspondentes de arqueas. Estas subunidades proteicas da RNase P compártense coa RNase MRP,[14][15][16] unha ribonucleoproteína catalítica implicada no procesamento de ARN ribosómico no nucléolo.[17] Non se demostrou que a RNase P dos eucariotas era un ribozima ata recentemente.[18] Por conseguinte, as numerosas subunidades proteicas da RNase P eucariota teñen unha contribución menor ao propio procesamento do ARNt,[19] pero parecen ser esenciais para a función da RNase P e RNase MRP noutros procesos bolóxicoas, como a transcrición de xenes e o ciclo celular.[3][20] Malia a orixe bacteriana das mitocondrias e cloroplastos, estes orgánulos nos animais superiores e plantas non parecen conter unha RNase P baseada no ARN. Demostrouse que a RNase P mitocondrial humana é unha proteína e non contén ARN (non é un ribozima).[21] A RNase P dos cloroplastos de espinacas funciona sen ter unha subunidade de ARN.[22]
Terapias que usan a RNase P
[editar | editar a fonte]A RNase P está estudándose agora como unha posible terapia para doenzas como a infección polo virus herpes simplex,[23] citomegalovirus,[23][24] gripe e outras infeccións respiratorias,[25] VIH-1[26] e o cancro causado polo xene de fusión BCR-ABL.[23][27] Fórmanse secuencias guía externas (EGSs) con complementariedade co ARMn oncoxénico viral e estruturas que imitan o bucle T e o talo aceptor do ARNt.[25] Estas estruturas permiten que a RNase P recoñeza as EGS e corte o ARNm diana. As terapias de EGS demostraro ser efectivas en cultivo e en ratos vivos.[28]
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 Guerrier-Takada C, Gardiner K, Marsh T, Pace N, Altman S (1983). "The RNA moiety of ribonuclease P is the catalytic subunit of the enzyme". Cell 35 (3 Pt 2): 849–57. PMID 6197186. doi:10.1016/0092-8674(83)90117-4.
- ↑ 2,0 2,1 Jarrous N, Reiner R (2007). "Human RNase P: a tRNA-processing enzyme and transcription factor". Nucleic Acids Res. 35 (11): 3519–24. PMC 1920233. PMID 17483522. doi:10.1093/nar/gkm071.
- ↑ 3,0 3,1 Reiner R, Ben-Asouli Y, Krilovetzky I, Jarrous N (2006). "A role for the catalytic ribonucleoprotein RNase P in RNA polymerase III transcription". Genes Dev. 20 (12): 1621–35. PMC 1482482. PMID 16778078. doi:10.1101/gad.386706.
- ↑ Evans D, Marquez SM, Pace NR (2006). "RNase P: interface of the RNA and protein worlds". Trends Biochem. Sci. 31 (6): 333–41. PMID 16679018. doi:10.1016/j.tibs.2006.04.007.
- ↑ Tsai, Hsin-Yue; Masquida, Benoît; Biswas, Roopa; Westhof, Eric; Gopalan, Venkat (2003-01-24). "Molecular modeling of the three-dimensional structure of the bacterial RNase P holoenzyme". Journal of Molecular Biology 325 (4): 661–675. ISSN 0022-2836. PMID 12507471. doi:10.1016/s0022-2836(02)01267-6.
- ↑ Reiter N, Osterman A, Torres-Larios A, Swinger KK, Pan T, Mondragon A, Nicholas J.; Osterman, Amy; Torres-Larios, Alfredo; Swinger, Kerren K.; Pan, Tao; Mondragón, Alfonso (2010). "Structure of a bacterial ribonuclease P holoenzyme in complex with tRNA". Nature 468 (7325): 784–789. Bibcode:2010Natur.468..784R. PMC 3058908. PMID 21076397. doi:10.1038/nature09516.
- ↑ Masquida B, Westhof E, B.; Westhof, E. (2011). "RNase P: At last, the key finds its lock". RNA 17 (9): 1615–1618. PMC 3162327. PMID 21803972. doi:10.1261/rna.2841511.
- ↑ Hall TA, Brown JW (2002). "Archaeal RNase P has multiple protein subunits homologous to eukaryotic nuclear RNase P proteins". RNA 8 (3): 296–306. PMC 1370252. PMID 12003490. doi:10.1017/S1355838202028492.
- ↑ Fukuhara H, Kifusa M, Watanabe M, Terada A, Honda T, Numata T, Kakuta Y, Kimura M (2006). "A fifth protein subunit Ph1496p elevates the optimum temperature for the ribonuclease P activity from Pyrococcus horikoshii OT3". Biochem. Biophys. Res. Commun. 343 (3): 956–64. PMID 16574071. doi:10.1016/j.bbrc.2006.02.192.
- ↑ Tsai HY, Pulukkunat DK, Woznick WK, Gopalan V (2006). "Functional reconstitution and characterization of Pyrococcus furiosus RNase P". Proc. Natl. Acad. Sci. U.S.A. 103 (44): 16147–52. Bibcode:2006PNAS..10316147T. PMC 1637551. PMID 17053064. doi:10.1073/pnas.0608000103.
- ↑ 11,0 11,1 Lai LB, Chan PP, Cozen AE, et al. (December 2010). "Discovery of a minimal form of RNase P in Pyrobaculum". Proc. Natl. Acad. Sci. U.S.A. 107 (52): 22493–8. Bibcode:2010PNAS..10722493L. PMC 3012483. PMID 21135215. doi:10.1073/pnas.1013969107.
- ↑ Randau L, Schröder I, Söll D (May 2008). "Life without RNase P". Nature 453 (7191): 120–3. Bibcode:2008Natur.453..120R. PMID 18451863. doi:10.1038/nature06833.
- ↑ Marquez SM, Chen JL, Evans D, Pace NR (2006). "Structure and Function of Eukaryotic Ribonuclease P RNA". Mol. Cell 24 (3): 445–56. PMC 1716732. PMID 17081993. doi:10.1016/j.molcel.2006.09.011.
- ↑ 14,0 14,1 Chamberlain JR, Lee Y, Lane WS, Engelke DR (1998). "Purification and characterization of the nuclear RNase P holoenzyme complex reveals extensive subunit overlap with RNase MRP". Genes Dev. 12 (11): 1678–90. PMC 316871. PMID 9620854. doi:10.1101/gad.12.11.1678.
- ↑ Salinas K, Wierzbicki S, Zhou L, Schmitt ME (2005). "Characterization and purification of Saccharomyces cerevisiae RNase MRP reveals a new unique protein component". J. Biol. Chem. 280 (12): 11352–60. PMID 15637077. doi:10.1074/jbc.M409568200.
- ↑ Welting TJ, Kikkert BJ, van Venrooij WJ, Pruijn GJ (2006). "Differential association of protein subunits with the human RNase MRP and RNase P complexes". RNA 12 (7): 1373–82. PMC 1484433. PMID 16723659. doi:10.1261/rna.2293906.
- ↑ Clayton DA (2001). "A big development for a small RNA". Nature 410 (6824): 29–31. PMID 11242026. doi:10.1038/35065191.
- ↑ Kikovska E, Svärd SG, Kirsebom LA (2007). "Eukaryotic RNase P RNA mediates cleavage in the absence of protein". Proc. Natl. Acad. Sci. U.S.A. 104 (7): 2062–7. PMC 1892975. PMID 17284611. doi:10.1073/pnas.0607326104.
- ↑ Willkomm DK, Hartmann RK (2007). "An important piece of the RNase P jigsaw solved". Trends Biochem. Sci. 32 (6): 247–50. PMID 17485211. doi:10.1016/j.tibs.2007.04.005.
- ↑ Gill T, Cai T, Aulds J, Wierzbicki S, Schmitt ME (2004). "RNase MRP Cleaves the CLB2 mRNA To Promote Cell Cycle Progression: Novel Method of mRNA Degradation". Mol. Cell. Biol. 24 (3): 945–53. PMC 321458. PMID 14729943. doi:10.1128/MCB.24.3.945-953.2004.
- ↑ J. Holzmann; P. Frank; E. Löffler; K. Bennett; C. Gerner; W. Rossmanith (2008). "RNase P without RNA: Identification and functional reconstitution of the human mitochondrial tRNA processing enzyme". Cell 135 (3): 462–474. PMID 18984158. doi:10.1016/j.cell.2008.09.013.
- ↑ B. C. Thomas; X. Li; P. Gegenheimer (2000). "Chloroplast ribonuclease P does not utilize the ribozyme-type pre-tRNA cleavage mechanism". RNA 6 (4): 545–553. PMC 1369935. PMID 10786845. doi:10.1017/S1355838200991465.
- ↑ 23,0 23,1 23,2 Trang, P; Kim, K; Liu, F (June 6, 2004). "Developing RNase P ribozymes for gene-targeting and antiviral therapy". Cell Microbiology 6 (6): 499–508. PMID 15104592. doi:10.1111/j.1462-5822.2004.00398.x.
- ↑ Trang, P; Kilani, A; Lee, J; Hsu, A; Liou, K; Kim, J; Nassi, A; Kim, K; Liu, F (August 25, 2002). "RNase P ribozymes for the studies and treatment of human cytomegalovirus infections". J Clin Virol S2: S63–74. PMID 12361758. doi:10.1016/s1386-6532(02)00097-5.
- ↑ 25,0 25,1 Dreyfus, David H.; Tompkins, S. Mark; Fuleihan, Ramsay; Ghoda, Lucy Y (2007). "Gene silencing in the therapy of influenza and other respiratory diseases: Targeting to RNase P by use of External Guide Sequences (EGS)". Biologics: Targets and Therapy 1 (4): 425–32. PMC 2721295. PMID 19707312.
- ↑ Zeng, WB; Chen, YC; Bai, Y; Trang, P; Vu, GP; Lu, SW; Wu, JG; Liu, FY (December 26, 2012). "Effective inhibition of Human Immunodeficiency Virus 1 replication by engineer RNase P ribozyme". PLOS ONE 7 (12): e51855. Bibcode:2012PLoSO...751855Z. PMC 3530568. PMID 23300569. doi:10.1371/journal.pone.0051855.
- ↑ Cobaleda, C; Sanchez-Garcia, I (2000). "In vivo inhibition by a site-specific catalytic RNA subunit of RNase P designed against the BCR-ABL oncogenic products: a novel approach for cancer treatment". Blood 95 (3): 731–7. PMID 10648380. doi:10.1182/blood.V95.3.731.003k28_731_737.
- ↑ Sawyer, AJ; Wesolowski, D; Gandotra, N; Stojadinovic, A; Izadjoo, M; Altman, S; Kyriakides, TR (2013). "A peptide-morpholino oligomer conjugate targeting Staphylococcus aureus gyrA mRNA improves healing in an infected mouse cutaneous wound model". Int. J. Pharm. 453 (2): 651–655. PMC 3756894. PMID 23727592. doi:10.1016/j.ijpharm.2013.05.041.
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Nobel Lecture of Sidney Altman, Nobel prize in Chemistry 1989
- Frank, DN; Pace NR (1998). "Ribonuclease P: unity and diversity in a tRNA processing ribozyme". Annu Rev Biochem 67: 153–180. PMID 9759486. doi:10.1146/annurev.biochem.67.1.153.
- Brown, JW (1999). "The Ribonuclease P Database". Nucleic Acids Res 27 (1): 314–. PMC 148169. PMID 9847214. doi:10.1093/nar/27.1.314.
Ligazóns externas
[editar | editar a fonte]- RNase P DatabaseArquivado 14 de maio de 2008 en Wayback Machine. en ncsu.edu
- Páxina para o RNase P nuclear en Rfam
- Páxina para o RNase P arqueana en Rfam
- Páxina para o RNase P bacteriana de clase A en Rfam
- Páxina para o RNase P bacteriana de clase B en Rfam
- RNase P Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- EC 3.1.26.5