O factor de crecemento endotelial vascular ou VEGF (do inglés vascular endothelial growth factor), antes chamado factor de permeabilidade vascular (VPF),[1] é unha proteína de sinalización producida polas células que estimula a vasculoxénese e a anxioxénese, favorecendo a formación de vasos sanguíneos. Forma parte do sistema que recupera a subministración de oxíxeno aos tecidos cando a circulación sanguínea é inadecuada. A concentración no soro sanguíneo de VEGF é alta na asma bronquial e diabetes mellitus.[2] A función normal do VEGF é crear novos vasos sanguíneos durante o desenvolvemento embrionario, e despois dunha lesión, no músculo despois do exercicio ou para xerar unha circulación colateral que sortee vasos bloqueados.
A sobreexpresión de VEGF pode contribuír ao desenvolvemento de doenzas. Os cancros sólidos non poden crecer alén dun tamaño limitado sen un rego sanguíneo axeitado; os cancros que poden expresar VEGF poden crecer e metastatizarse. A sobreexpresión de VEGF pode causar doenzas vasculares na retina do ollo e outras partes do corpo. Fármacos como o bevacizumab e ranibizumab poden inhibir o VEGF e controlar ou facer máis lentas esas doenzas.
O VEGF é unha subfamilia de factores de crecemento, concretamente a familia do factor de crecemento derivado de plaquetas dos factores de crecemento de nó de cistina. Son importantes proteínas de sinalización implicadas tanto na vasculoxénese (formación de novo dos vasos do sistema ciruclatorio embrional) coma na anxioxénese (crecemento de vasos nunha vasculatura xa existente).
Historia
[editar | editar a fonte]O VEGF foi identificado inicialmente en cobaias, hámsteres, e ratos por Senger et al. en 1983.[1] Foi purificado e clonado por Ferrara e Henzel en 1989.[3] O splicing alternativo do VEGF descubriuno Tischer et al. en 1991.[4] Entre 1996 e 1997, Christinger e De Vos obtiveron a estrutura cristalina do VEGF, primeiro a unha resolución de 2,5 Å e despois a 1,9 Å.[5][6][7]
En 1992 Ferrara et al. demostraron que a tirosina quinase-1 de tipo Fms (flt-1) era o receptor do VEGF.[8] En 1992 Terman et al. demostraron que o receptor de dominio de inserción de quinase (KDR) era un receptor de VEGF.[9] En 1998, demostrouse que a neuropilina 1 e a neuropilina 2 actuaban como receptores de VEGF.[10]
Clasificación
[editar | editar a fonte]
A familia do VEGF comprende en mamíferos cinco membros: VEGF-A, factor de crecemento placentario (PGF), VEGF-B, VEGF-C e VEGF-D. Os últimos foron descubertos despois de VEGF-A, e anteriromente, cando VEG-A era o único coñecido, chamábase simplemente VEGF. Descubríronse tamén varias proteínas relacionadas don VEGF codificadas por virus (VEGF-E) e atopadas no veleno de serpes (VEGF-F).
| Tipo | Función |
|---|---|
| VEGF-A |
|
| VEGF-B | Anxioxénese embrional (concretamente no tecido miocárdico)[11] |
| VEGF-C | Linfanxioxénese |
| VEGF-D | Necesario para o desenvolvemento dos vasos linfáticos que rodean os bronquíolos |
| PlGF | Importante para a vasculoxénese, e tamén necesario para a anxioxénese durante a isquemia, inflamación, curación de feridas e cancro. |
A actividade de VEGF-A, como o seu nome indica, foi estudada principalmente en células do endotelio vascular, aínda que ten efectos noutros tipos celulares (por exemplo, estimulación da migración de monocitos/macrófagos, neuronas, células cancerosas, células epiteliais dos riles). In vitro, o VEGF-A estimula a mitoxénese das células endoteliais e a migración celular. O VEGF-A é tamén un vasodilatador e incrementa a permeabilidade microvascular e foi denominado orixinalmente factor de permeabilidade vascular.
Isoformas
[editar | editar a fonte]
Hai moitas isoformas do VEGF-A que son o resultado do splicing alternativo do ARNm dun só xene VEGFA de 8 exóns. Clasifícanse en dous grupos que se nomean de acordo co seu sitio de empalme (splicing) do seu exón terminal (o exón 8): o sitio de empalme proximal (denominado VEGFxxx) ou o distal (VEGFxxxb). Ademais, o splicing alternativo dos exóns 6 e 7 altera a súa afinidade de unión á heparina e o número de aminoácidos (en humanos: VEGF121, VEGF121b, VEGF145, VEGF165, VEGF165b, VEGF189, VEGF206; os ortólogos en roedores destas proteínas conteñen un aminoácido menos). Estes dominios teñen importantes consecuencias funcionais para as variantes de empalme de VEGF, xa que o sitio de empalme terminal (no exón 8) determina se as proteínas son pro-anxioxénicas (sitio de empalme proximal, expresado durante a anxioxénese) ou anti-anxioxénicas (sitio de empalme distal, expresado en tecidos normais). Ademais, a inclusión ou exclusión dos exóns 6 e 7 media as interaccións co proteoglicano heparán sulfato (HSPG) e o correceptor neuropilina da superficie celular, potenciando a súa capacidade de unirse e activar os receptores de VEGF (VEGFRs).[12] Recentemente, demostrouse que o VEGF-C é un importante indutor da neuroxénese na zona subventricular murina, sen exercer efectos anxioxénicos.[13]
Mecanismo
[editar | editar a fonte]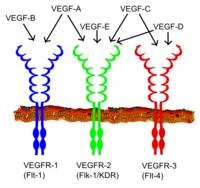
Todos os membros da familia VEGF estimulan as respostas celulares ao unirse a receptores de tirosina quinase (os VEGFRs) da superficie celular, causándolles que se dimericen e se activen por transfosforilación, aínda que en difernttes sitios, tempos e extensión. Os receptores VEGF teñen unha porción extracelular que consta de 7 dominios de tipo inmunoglobulina, unha soa rexión transmembrana, e unha porción intracelular que contén un dominio de tirosina-quinase. O VEGF-A únese a VEGFR-1 (Flt-1) e VEGFR-2 (KDR/Flk-1).[15] O VEGFR-2 parece mediar case todas as respostas celulares coñecidas do VEGF. A función de VEGFR-1 está peor definida, aínda que se cre que modula a sinalización de VEGFR-2.[16] Outra función de VEGFR-1 pode ser actuar como un receptor reclamo, secuestrando VEGF evitando a súa unión a VEGFR-2 (isto parece ser especialmente importante durante a vasculoxénese no embrión). O VEGF-C e o VEGF-D, pero non VEGF-A, son ligandos dun terceiro receeptor (VEGFR-3/Flt4), que media a linfanxioxénese. O receptor (VEGFR3) é o sitio de unión dos principais ligandos (VEGFC e VEGFD), os cales median a perpetua acción e función de ligandos nas células diana. O VEGF-C pode estimular a linfanxioxénese (vía VEGFR3) e a anxioxénese vía VEGFR2. O VEGF-R3 detectouse en células endoteliais linfáticas no corpo lúteo de moitas especies, vacas, búfalos de auga e primates.[17]
Expresión
[editar | editar a fonte]A produción de VEGF-A pode ser inducida en células que non están recibindo oxíxeno dabondo.[15] Cando unha célula ten deficiencia de oxíxeno, produce HIF (factor inducible por hipoxia), que é un factor de transcrición. O HIF estimula a liberación de VEGF-A, entre outras funcións (incluíndo a modulación da eritropoese). O VEGF-A circulante únese despois a receptores de VEGF das células endoteliais, desencadeando unha vía de tirosina quinase que leva á anxioxénese. A expresión de anxiopoetina-2 en ausencia de VEGF leva á morte da célula endotelial e á regresión vascular.[18] Inversamente, un estudo alemán feito in vivo atopou que as concentracións de VEGF en realidade decrecen despois dun 25% de redución da captación de oxíxeno durante 30 minutos.[19] O HIF1 alfa e o HIF1 beta están sendo producidos constantemente pero o HIF1 alfa é altamente lábil en presenza de O2, así que, en condicións aeróbicas, é degradado. Cando a célula queda en situación hipóxica, o HIF1 alfa persiste e o complexo HIF1 alfa/beta estimula a liberación de VEGF.
Importancia clínica
[editar | editar a fonte]O VEGF en enfermidades
[editar | editar a fonte]O VEGF-A foi implicado en prognósticos de maior gravidade no cancro de mama. Numerosos estudos mostran unha diminución da supervivnecia global e da supervivencia libre de enfermidade nos pacientes con tumores que sobreexpresan o VEGF. A sobreexpresión de VEGF-A pode ser un paso inicial no proceso de formación de metástases, un paso que está implicado no cambio "anxioxénico". Aínda que o VEGF-A foi correclacionado cunha peor supervivencia, o seu mecanismo exacto de acción na progresión dos tumores non está claro.
O VEGF-A tamén se libera na artrite reumatoide en resposta ao TNF-α, incrmentando o inchamento e permeabilidade endotelial e tamén estimulando a anxioxénese (formación de capilares).
O VEGF-A é tamén importante na retinopatía diabética. Os problemas microcirculatorios na retina de persoas con diabetes pode causar isquemia retinal, que ten como resultado a liberación de VEGF-A, e un cambio no balance das isoformas VEGFxxx proanxioxénicas con respecto ás isoformas normalmente expresadas VEGFxxxb. O VEGFxxx pode despois causar a creación de novos vasos sanguíneos na retina e noutras partes do ollo, anunciando cambios que poden levar a perder a vista.
O VEGF-A xoga un papel na patoloxía da forma húmida da dexeneración macular relacionada coa idade (AMD), que é a principal causa de cegueira nas persoas vellas nos países industrializados. A patoloxía vascular da AMD comparte certas similitudes coa retinopatía diabética, aínda que a causa da enfermidade e a fonte típica de neovascularización difire nas dúas enfermidades.
Os niveis no soro de VEGF-D están significativamente elevados en pacientes con anxiosarcoma.[20]
Unha vez liberado, o VEGF-A pode orixinar varias respostas. Pode causar que unha célula sobreviva, se mova, ou se diferencie máis. Xa que logo, o VEGF é unha diana potencial para o tratamento do cancro. O primeiro fármaco anti-VEGF, un anticorpo monoclonal denominado bevacizumab, aprobouse en 2004. Aproximadamente o 10-15% dos pacientes benefícianse da terapia con bevacizumab; porén, os biomarcadores para a eficacia do bevacizumab non se coñecen aínda.
Estudos actuais inican que os VEGFs non son os únicos promotores da anxioxénese. En concreto, FGF2 e HGF son tamén potentes factores anxioxénicos.
Os pacientes que sofren enfisema pulmonar presentan unha diminución dos niveis de VEGF nas arterias pulmonares.
Nos riles, o incremento da expresión de VEGF-A nos glomérulos causa directamente a hipertrofia glomerular que está asociada con proteinuria.[21]
As alteracións do VEGF poden predicir a pre-eclampsia de comezo temperán.[22]
Terapias anti-VEGF
[editar | editar a fonte]As terapias anti-VEGF son importantes no tratamento de certos cancros e na dexeneración macular relacionada coa idade. Poden consistir no uso de anticorpos monoclonais como bevacizumab (Avastin), derivados de anticorpos como ranibizumab (Lucentis), ou pequenas moléculas de administración oral que inhiben as tirosina quinases estimuladas polo VEGF: lapatinib (Tykerb/Tyverb), sunitinib (Sutent), sorafenib (Nexavar), axitinib, e pazopanib. (Algunhas destas terapias teñen como diana os receptores de VEGF en vez dos propios VEGFs.) O THC e o cannabidiol inhiben o VEGF e fan máis lento o crecemento de gliomas. Ambos os compostos baseados en anticorpos e os dispoñibles por vía oral son xa comercializados, pero a axitinib e pazopanib están aínda en ensaios clínicos.
Bergers e Hanahan concluíron en 2008 que os fármacos anti-VEGF poden mostrar eficacia terapéutica en modelos de ratos do cancro e nun crecente número de cancros humanos. Pero, "os beneficios son como moito transitorios e van seguidos da restauración do crecemento do tumor e da súa progresión."[23]
Os últimos estudos sobre as consecuencias do uso de inhibidores do VEGF indican que, aínda que poden reducir o crecemento de tumores primarios, os inhibidores do VEGF poden á vez promover a invasividade e metástase dos tumores.[24][25]
O AZ2171 (cediranib), que é un inhibidor da tirosina quinase de dianas múltiples ten efectos anti-edema ao reducir a permeabilidde e axudar á normalización vascular.
En 2014 unha Revisión Sistemática Cochrane estudou a efectividade do ranibizumab e o pegaptanib, en pacientes que sofren edema macular causado por oclusión da vea retinal central.[26] Os participantes nos dous grupos de tratamento estudados mostraron melloras nas medidas de agudeza visual e na redución dos síntomas de edema macular en seis meses.[26]
Ensaios pre-clínicos
[editar | editar a fonte]O VEGF é tamén inhibido polas tiazolidinadionas (usadas para a diabetes mellitus tipo 2 e doenzas relacionadas), e o seu efecto sobre as células granulosas dálle ás tiazolidinadionas o potencial de ser usadas na síndrome de hiperestimulación ovárica.[27]
Dexeneración macular relacionada coa idade neovascular
[editar | editar a fonte]Ranibizumab é un fragmento de anticorpo monoclonal (Fab) derivado do bevacizumab, que foi desenvolvido por Genetech para o seu uso intraocular. En 2006, a FDA aprobou o fármaco para o tratamento de dexeneración macular relacionada coa idade neovascular (AMD húmida). Daquela o fármaco sometérase a tres ensaios clínicos con éxito.[28]
En 2006 publicouse que as inxeccións intravítreas mensuais de ranibizumab levaron a un incremento significativo do nivel da agudeza visula media comparada co dunha inxección simulada. Chegouse á conclusión no estudo de dous anos en fase III que o ranibizumab é moi efectivo no tratamento da AMD minimamente clásica (MC) ou AMD húmida oculta (dexeneración macular relacionada coa idade) con taxas baixas de efectos adversos oculares.[29]
Outro estudo publicado en 2009 proporciona probas da eficacia do ranibizumab. A inxecciónn intravítrea mensual de ranibizumab causa un incremento significativo no nivel de agudeza visual media comparado co da terapia fotodinámica con verteporfina. A conclusión do estudo de dous anos en fase III foi que o ranibizumab era superior á terapia fotodinámica con verteporfina no tratamento da AMD húmida predominantemente clásica (PC) con taxs baixas de efectos adversos oculares.[30]
Porén, o custo/efectividade do ranibizumab é cuestionado debido o seu enorme prezo. Cada inxección costa 2 millóns de dólares e deben administrarse mensualmente. Unha alternativa moito máis barata é o bevaciazumab.
En 2007, publicouse que, a menos que o ranibizumab sexa 2,5 veces máis efectivo que o bevacizumab, o ranibizumab non terá un beneficio custo/efectividade. Concluíuse que o prezo do fármaco tería que ser reducido drasticamente para que puidese ter un beneficio custo/efectividade.[31]
En 2012, o tratamento anti-VEGF con Avastin foi aceptado por Medicare, e ten un prezo e eficacia razoables. Lucentis ten unha estrutura similar pero máis pequena que a Avastin, e está aprobado pola FDA pero é máis caro, como tamén o é EYLEA (aflibercept). Están a realizarse ensaios comparativos sobre a eficacia destes tratamentos.
Efectos neurolóxicos do VEGF durante o exercicio
[editar | editar a fonte]A hipoxia regula á alza fortemente a expresión de VEGF e este exerce un efecto neuroprotector sobre as neuronas hipóxicas.[32] O exercicio aeróbico incrementa a biosíntese de VEGF nos tecidos periféricos, que despois cruza a barreira hematoencefálica e promove a neuroxénese e anxioxénese no sistema nervioso central.[33][34][35] Os incrementos inducidos polo exercicio na sinalización por VEGF melloran o volume sanguíneo cerebral e contribúen á neuroxénese inducida polo exercicio no hipocampo.[34][35][36]
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 Senger, DR; Galli, SJ; Dvorak, AM; Perruzzi, CA; Harvey, VS; Dvorak, HF (25 February 1983). "Tumor cells secrete a vascular permeability factor that promotes accumulation of ascites fluid.". Science 219 (4587): 983–5. PMID 6823562. doi:10.1126/science.6823562.
- ↑ Cooper, Mark; Dimitria Vranes; Sherif Youssef; Steven A. Stacker; Alison J. Cox; Bishoy Rizkalla; David J. Casley; Leon A. Bach; Darren J. Kelly; Richard E. Gilbert (November 1999). "Increased Renal Expression of Vascular Endothelial Growth Factor (VEGF) and Its Receptor VEGFR-2 in Experimental Diabetes" (PDF). Diabetes 48 (11): 2229–2239. doi:10.2337/diabetes.48.11.2229. Consultado o 6 November 2013.
- ↑ Ferrara, N; Henzel, WJ (15 June 1989). "Pituitary follicular cells secrete a novel heparin-binding growth factor specific for vascular endothelial cells.". Biochemical and Biophysical Research Communications 161 (2): 851–8. PMID 2735925. doi:10.1016/0006-291x(89)92678-8.
- ↑ Tischer, E; Mitchell, R; Hartman, T; Silva, M; Gospodarowicz, D; Fiddes, JC; Abraham, JA (25 June 1991). "The human gene for vascular endothelial growth factor. Multiple protein forms are encoded through alternative exon splicing.". The Journal of Biological Chemistry 266 (18): 11947–54. PMID 1711045.
- ↑ Christinger, Hans W.; Muller, Yves A.; Berleau, Lea T.; Keyt, Bruce A.; Cunningham, Brian C.; Ferrara, Napoleone; de Vos, Abraham M. (November 1996). "Crystallization of the receptor binding domain of vascular endothelial growth factor". Proteins: Structure, Function, and Genetics 26 (3): 353–357. doi:10.1002/(SICI)1097-0134(199611)26:3<353::AID-PROT9>3.0.CO;2-E.
- ↑ Muller, YA; Li, B; Christinger, HW; Wells, JA; Cunningham, BC; de Vos, AM (8 July 1997). "Vascular endothelial growth factor: crystal structure and functional mapping of the kinase domain receptor binding site.". Proceedings of the National Academy of Sciences of the United States of America 94 (14): 7192–7. PMID 9207067. doi:10.1073/pnas.94.14.7192.
- ↑ Muller, YA; Christinger, HW; Keyt, BA; de Vos, AM (15 October 1997). "The crystal structure of vascular endothelial growth factor (VEGF) refined to 1.93 A resolution: multiple copy flexibility and receptor binding.". Structure (London, England: 1993) 5 (10): 1325–38. PMID 9351807. doi:10.1016/s0969-2126(97)00284-0.
- ↑ de Vries, C; Escobedo, JA; Ueno, H; Houck, K; Ferrara, N; Williams, LT (21 February 1992). "The fms-like tyrosine kinase, a receptor for vascular endothelial growth factor.". Science 255 (5047): 989–91. PMID 1312256. doi:10.1126/science.1312256.
- ↑ Terman, BI; Dougher-Vermazen, M; Carrion, ME; Dimitrov, D; Armellino, DC; Gospodarowicz, D; Böhlen, P (30 September 1992). "Identification of the KDR tyrosine kinase as a receptor for vascular endothelial cell growth factor.". Biochemical and Biophysical Research Communications 187 (3): 1579–86. PMID 1417831. doi:10.1016/0006-291x(92)90483-2.
- ↑ Soker, S; Takashima, S; Miao, HQ; Neufeld, G; Klagsbrun, M (20 March 1998). "Neuropilin-1 is expressed by endothelial and tumor cells as an isoform-specific receptor for vascular endothelial growth factor.". Cell 92 (6): 735–45. PMID 9529250. doi:10.1016/s0092-8674(00)81402-6.
- ↑ Claesson-Welsh, L. (20 August 2008). "VEGF-B Taken to Our Hearts: Specific Effect of VEGF-B in Myocardial Ischemia". Arteriosclerosis, Thrombosis, and Vascular Biology 28 (9): 1575–1576. doi:10.1161/ATVBAHA.108.170878.
- ↑ "A VEGF-A splice variant defective for heparan sulfate and neuropilin-1 binding shows attenuated signaling through VEGFR-2". Cellular and Molecular Life Sciences 63: 2067–2077. doi:10.1007/s00018-006-6254-9.
- ↑ Shin, Y. J.; Choi, J. S.; et al. (2010). "Induction of vascular endothelial growth factor receptor-3 mRNA in glial cells following focal cerebral ischemia in rats". J Neuroimmunol 229 (1-2): 81–90. doi:10.1016/j.jneuroim.2010.07.008.
- ↑ "cancerpublications.com.". Arquivado dende o orixinal o 20 de abril de 2012. Consultado o 06 de agosto de 2015.
- ↑ 15,0 15,1 Holmes, Katherine; Roberts, Owain Ll; Thomas, Angharad M.; Cross, Michael J. (2007). "Vascular endothelial growth factor receptor-2: Structure, function, intracellular signalling and therapeutic inhibition". Cellular Signalling 19 (10): 2003–12. PMID 17658244. doi:10.1016/j.cellsig.2007.05.013.
- ↑ Karkkainen, M.J.; Petrova, T.V. (2000). "Vascular endothelial growth factor receptors in the regulation of angiogenesis and lymphangiogenesis". Oncogene 19 (49): 5598–5605. PMID 11114740. doi:10.1038/sj.onc.1203855.
- ↑ Ali, Ibne; et al. (2013). "Expression and localization of locally produced growth factors regulating lymphangiogenesis during different stages of the estrous cycle in corpus luteum of buffalo" (Bubalus bubalis)". Theriogenology 81: 428–436. doi:10.1016/j.theriogenology.2013.10.017.
- ↑ Harmey, Judith (2004). VEGF and cancer. Georgetown, Tex: Landes Bioscience/Eurekah.com New York, N.Y. Kluwer Academic/Plenum Publishers. ISBN 0-306-47988-5.
- ↑ Oltmanns, K. M.; Gehring, H; Rudolf, S; Schultes, B; Hackenberg, C; Schweiger, U; Born, J; Fehm, H. L.; Peters, A (2006). "Acute hypoxia decreases plasma VEGF concentration in healthy humans". AJP: Endocrinology and Metabolism 290 (3): E434–9. doi:10.1152/ajpendo.00508.2004. PMID 16219663.
- ↑ Amo, Y.; Masuzawa, M.; Hamada, Y.; Katsuoka, K. (2004). "Serum concentrations of vascular endothelial growth factor-D in angiosarcoma patients". British Journal of Dermatology 150 (1): 160–1. PMID 14746640. doi:10.1111/j.1365-2133.2004.05751.x.
- ↑ Liu, E.; Morimoto, M.; Kitajima, S.; Koike, T.; Yu, Y.; Shiiki, H.; Nagata, M.; Watanabe, T.; Fan, J. (2007). "Increased Expression of Vascular Endothelial Growth Factor in Kidney Leads to Progressive Impairment of Glomerular Functions". Journal of the American Society of Nephrology 18 (7): 2094–104. PMID 17554151. doi:10.1681/ASN.2006010075.
- ↑ Andraweera, P. H.; Dekker, G. A.; Roberts, C. T. (2012). "The vascular endothelial growth factor family in adverse pregnancy outcomes". Human Reproduction Update 18 (4): 436–457. doi:10.1093/humupd/dms011. PMID 22495259.
- ↑ Bergers G, Hanahan D (August 2008). "Modes of resistance to anti-angiogenic therapy". Nat. Rev. Cancer 8 (8): 592–603. PMC 2874834. PMID 18650835. doi:10.1038/nrc2442.
- ↑ Ebos, John; Christina R. Lee; William Cruz-Munoz; Georg A. Bjarnason; James G. Christensen; Robert S. Kerbel (March 2009). "Accelerated Metastasis after Short-Term Treatment with a Potent Inhibitor of Tumor Angiogenesis". Cancer Cell 15 (3): 232–239. PMID 19249681. doi:10.1016/j.ccr.2009.01.021. Consultado o 22 October 2012.
- ↑ Pàez-Ribes, Marta; Allen, Elizabeth; Hudock, James; Takeda, Takaaki; Okuyama, Hiroaki; Viñals, Francesc; Inoue, Masahiro; Bergers, Gabriele; Hanahan, Douglas; Casanovas, Oriol (March 2009). "Antiangiogenic Therapy Elicits Malignant Progression of Tumors to Increased Local Invasion and Distant Metastasis". Cancer Cell 15 (3): 220–231. PMC 2874829. PMID 19249680. doi:10.1016/j.ccr.2009.01.027. Consultado o 22 October 2012.
- ↑ 26,0 26,1 Braithwaite T, Nanji AA, Greenberg PB (2010). "Anti-vascular endothelial growth factor for macular edema secondary to central retinal vein occlusion". Cochrane Database Syst Rev 10: CD007325. PMID 20927757. doi:10.1002/14651858.CD007325.pub3.
- ↑ Shah DK, Menon KM, Cabrera LM, Vahratian A, Kavoussi SK, Lebovic DI (April 2010). "Thiazolidinediones decrease vascular endothelial growth factor (VEGF) production by human luteinized granulosa cells in vitro". Fertil. Steril. 93 (6): 2042–7. PMC 2847675. PMID 19342033. doi:10.1016/j.fertnstert.2009.02.059.
- ↑ "FDA Approves New Biologic Treatment for Wet Age-Related Macular Degeneration". FDA News & Events. June 30, 2006. Consultado o 17 April 2013.
- ↑ Brown, David M.; Michels, Mark; Kaiser, Peter K.; Heier, Jeffrey S.; Sy, Judy P.; Ianchulev, Tsontcho; Anchor Study, Group (2009). "Ranibizumab versus Verteporfin Photodynamic Therapy for Neovascular Age-Related Macular Degeneration: Two-Year Results of the ANCHOR Study". Ophthalmology 116 (1): 57–65. PMID 19118696. doi:10.1016/j.ophtha.2008.10.018.
- ↑ Rosenfeld, Philip J.; Brown, David M.; Heier, Jeffrey S.; Boyer, David S.; Kaiser, Peter K.; Chung, Carol Y.; Kim, Robert Y.; Marina Study, Group (2006). "Ranibizumab for Neovascular Age-Related Macular Degeneration". New England Journal of Medicine 355 (14): 1419–31. PMID 17021318. doi:10.1056/NEJMoa054481.
- ↑ Raftery, J.; Clegg, A.; Jones, J.; Tan, S. C.; Lotery, A. (2007). "Ranibizumab (Lucentis) versus bevacizumab (Avastin): modelling cost effectiveness". British Journal of Ophthalmology 91 (9): 1244–6. PMC 1954941. PMID 17431015. doi:10.1136/bjo.2007.116616.
- ↑ Malenka RC, Nestler EJ, Hyman SE (2009). Sydor A, Brown RY, ed. Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 221, 412. ISBN 978-0-07-148127-4.
- ↑ Tarumi T, Zhang R (January 2014). "Cerebral hemodynamics of the aging brain: risk of Alzheimer disease and benefit of aerobic exercise". Front Physiol 5: 6. PMC 3896879. PMID 24478719. doi:10.3389/fphys.2014.00006.
- ↑ 34,0 34,1 Silverman MN, Deuster PA (October 2014). "Biological mechanisms underlying the role of physical fitness in health and resilience". Interface Focus 4 (5): 20140040. doi:10.1098/rsfs.2014.0040. PMID 25285199
- ↑ 35,0 35,1 Bouchard J, Villeda SA (2015). "Aging and brain rejuvenation as systemic events". J. Neurochem. 132 (1): 5–19. PMC 4301186. PMID 25327899. doi:10.1111/jnc.12969.
- ↑ Gomez-Pinilla F, Hillman C (January 2013). "The influence of exercise on cognitive abilities". Compr Physiol 3 (1): 403–428. doi:10.1002/cphy.c110063. PMC 3951958. PMID 23720292.
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Bengoetxea H, Argandoña EG, Lafuente JV (2008). "Effects of Visual Experience on Vascular Endothelial Growth Factor Expression during the Postnatal Development of the Rat Visual Cortex". Cerebral Cortex. 18 (7): 1630–39. PMC 2430152. PMID 17986606. doi:10.1093/cercor/bhm190.
- Zan L, Wu H, Jiang J, Zhao S, Song Y, Teng G, Li H, Jia Y, Zhou M, Zhang X, Qi J, Wang J. (2011). "Temporal profile of Src, SSeCKS, and angiogenic factors after focal cerebral ischemia: correlations with angiogenesis and cerebral edema". Neurochem Int. 58 (8): 872–9. PMC 3100427. PMID 21334414. doi:10.1016/j.neuint.2011.02.014.
- Zan L, Zhang X, Xi Y, Wu H, Song Y, Teng G, Li H, Qi J, Wang J. (2014). "Src regulates angiogenic factors and vascular permeability after focal cerebral ischemia-reperfusion". Neuroscience. 262: 118–28. PMC 3943922. PMID 24412374. doi:10.1016/j.neuroscience.2013.12.060.
- Wang J, Fu X, Jiang C, Yu L Wang M, Han W, Liu L, Wang J. (2014). "Bone marrow mononuclear cell transplantation promotes therapeutic angiogenesis via upregulation of the VEGF-VEGFR2 signaling pathway in a rat model of vascular dementia". Behav Brain Res. 265: 171–80. PMC 4000455. PMID 24589546. doi:10.1016/j.bbr.2014.02.033.
- Ferrara N, Gerber HP (2002). "The role of vascular endothelial growth factor in angiogenesis". Acta Haematol. 106 (4): 148–56. PMID 11815711. doi:10.1159/000046610.
- Orpana A, Salven P (2003). "Angiogenic and lymphangiogenic molecules in hematological malignancies". Leuk. Lymphoma 43 (2): 219–24. PMID 11999550. doi:10.1080/10428190290005964.
- Afuwape AO, Kiriakidis S, Paleolog EM (2003). "The role of the angiogenic molecule VEGF in the pathogenesis of rheumatoid arthritis". Histol. Histopathol. 17 (3): 961–72. PMID 12168808.
- de Bont ES, Neefjes VM, Rosati S, et al. (2003). "New vessel formation and aberrant VEGF/VEGFR signaling in acute leukemia: does it matter?". Leuk. Lymphoma 43 (10): 1901–9. PMID 12481883. doi:10.1080/1042819021000015844.
- Ria R, Roccaro AM, Merchionne F, et al. (2003). "Vascular endothelial growth factor and its receptors in multiple myeloma". Leukemia 17 (10): 1961–6. PMID 14513045. doi:10.1038/sj.leu.2403076.
- Caldwell RB, Bartoli M, Behzadian MA, et al. (2004). "Vascular endothelial growth factor and diabetic retinopathy: pathophysiological mechanisms and treatment perspectives". Diabetes Metab. Res. Rev. 19 (6): 442–55. PMID 14648803. doi:10.1002/dmrr.415.
- Patan S (2004). "Vasculogenesis and angiogenesis". Cancer Treat. Res. Cancer Treatment and Research 117: 3–32. ISBN 978-1-4020-7704-3. PMID 15015550. doi:10.1007/978-1-4419-8871-3_1.
- Machein MR, Plate KH (2004). "Role of VEGF in developmental angiogenesis and in tumor angiogenesis in the brain". Cancer Treat. Res. Cancer Treatment and Research 117: 191–218. ISBN 978-1-4020-7704-3. PMID 15015562. doi:10.1007/978-1-4419-8871-3_13.
- Eremina V, Quaggin SE (2004). "The role of VEGF-A in glomerular development and function". Curr. Opin. Nephrol. Hypertens. 13 (1): 9–15. PMID 15090854. doi:10.1097/00041552-200401000-00002.
- Storkebaum E, Lambrechts D, Carmeliet P (2004). "VEGF: once regarded as a specific angiogenic factor, now implicated in neuroprotection". BioEssays 26 (9): 943–54. PMID 15351965. doi:10.1002/bies.20092.
- Ribatti D (2005). "The crucial role of vascular permeability factor/vascular endothelial growth factor in angiogenesis: a historical review". Br. J. Haematol. 128 (3): 303–9. PMID 15667531. doi:10.1111/j.1365-2141.2004.05291.x.
- Loureiro RM, D'Amore PA (2005). "Transcriptional regulation of vascular endothelial growth factor in cancer". Cytokine Growth Factor Rev. 16 (1): 77–89. PMID 15733833. doi:10.1016/j.cytogfr.2005.01.005.
- Herbst RS, Onn A, Sandler A (2005). "Angiogenesis and lung cancer: prognostic and therapeutic implications". J. Clin. Oncol. 23 (14): 3243–56. PMID 15886312. doi:10.1200/JCO.2005.18.853.
- Pufe T, Kurz B, Petersen W, et al. (2006). "The influence of biomechanical parameters on the expression of VEGF and endostatin in the bone and joint system". Ann. Anat. 187 (5–6): 461–72. PMID 16320826. doi:10.1016/j.aanat.2005.06.008.
- Tong JP, Yao YF (2006). "Contribution of VEGF and PEDF to choroidal angiogenesis: a need for balanced expressions". Clin. Biochem. 39 (3): 267–76. PMID 16409998. doi:10.1016/j.clinbiochem.2005.11.013.
- Lambrechts D, Carmeliet P (2007). "VEGF at the neurovascular interface: therapeutic implications for motor neuron disease". Biochim. Biophys. Acta 1762 (11–12): 1109–21. PMID 16784838. doi:10.1016/j.bbadis.2006.04.005.
- Matsumoto T, Mugishima H (2006). "Signal transduction via vascular endothelial growth factor (VEGF) receptors and their roles in atherogenesis". J. Atheroscler. Thromb. 13 (3): 130–5. PMID 16835467. doi:10.5551/jat.13.130.
- Bogaert E, Van Damme P, Van Den Bosch L, Robberecht W (2006). "Vascular endothelial growth factor in amyotrophic lateral sclerosis and other neurodegenerative diseases". Muscle Nerve 34 (4): 391–405. PMID 16856151. doi:10.1002/mus.20609.
- Mercurio AM, Lipscomb EA, Bachelder RE (2006). "Non-angiogenic functions of VEGF in breast cancer". Journal of Mammary Gland Biology and Neoplasia 10 (4): 283–90. PMID 16924371. doi:10.1007/s10911-006-9001-9.
- Makinde T, Murphy RF, Agrawal DK (2007). "Immunomodulatory role of vascular endothelial growth factor and angiopoietin-1 in airway remodeling". Curr. Mol. Med. 6 (8): 831–41. PMID 17168735. doi:10.2174/156652406779010795.
- Rini BI, Rathmell WK (2007). "Biological aspects and binding strategies of vascular endothelial growth factor in renal cell carcinoma". Clin. Cancer Res. 13 (2 Pt 2): 741s–746s. PMID 17255303. doi:10.1158/1078-0432.CCR-06-2110.
- Rodgers LS, Lalani S, Hardy KM, Xiang X, Broka D, Antin PB, Camenisch TD. (2006). "Depolymerized hyaluronan induces vascular endothelial growth factor, a negative regulator of developmental epithelial-to-mesenchymal transformation". Circ Res. 99 (6): 583–9. PMID 16931798. doi:10.1161/01.RES.0000242561.95978.43.
- Qaum, T; Xu, Q; Joussen, AM; et al. (2001). "VEGF-initiated blood-retinal barrier breakdown in early diabetes". Invest Ophthalmol Vis Sci 42: 2408–2413.
Ligazóns externas
[editar | editar a fonte]- Vascular Endothelial Growth Factors Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- Proteopedia Vascular_Endothelial_Growth_Factor - Estrutura en 3 D interactiva do VEGF