| Adenilato quinase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
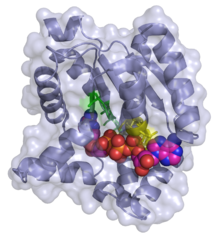 Modelo 3D de fitas/superficie da adenilato quinase en complexo coa bis(adenosín)tetrafosfato (ADP-ADP) | |||||||||
| Identificadores | |||||||||
| Símbolo | ADK | ||||||||
| Pfam | PF00406 | ||||||||
| InterPro | IPR000850 | ||||||||
| PROSITE | PDOC00104 | ||||||||
| SCOPe | 1ake / SUPFAM | ||||||||
| |||||||||
A adenilato quinase (EC 2.7.4.3), tamén chamada ADK ou mioquinase, é un encima fosfotransferase que cataliza a interconversión dos varios fosfatos de adenosina (ATP, ADP e AMP). A ADK monitoriza constantemente os niveis de nucleótidos fosfato dentro da célula e xoga un importante papel na homeostase da enerxía celular.
| Adenilato quinase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
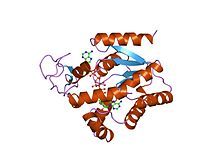 Adenilato quinase de Bacillus stearothermophilus | |||||||||
| Identificadores | |||||||||
| Símbolo | ADK_lid | ||||||||
| Pfam | PF05191 | ||||||||
| InterPro | IPR007862 | ||||||||
| PROSITE | PDOC00104 | ||||||||
| SCOPe | 1ake / SUPFAM | ||||||||
| |||||||||
| Adenilato quinase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Número EC | 2.7.4.3 | ||||||||
| Número CAS | 2598011 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| |||||||||
A reacción catalizada é:
A constante de equilibrio varía coas condicións, pero está preto de 1.[1] Así, a ΔGo para esta reacción está próxima a cero. No músculo de diversas especies de vertebrados e invertebrados, a concentración de ATP é normalmente de 7 a 10 veces maior que a de ADP, e xeralmente 100 veces maior que a de AMP.[2] A velocidade da fosforilación oxidativa está controlada pola dispoñibilidade de ADP. Así, a mitocondria intenta manter os niveis de ATP altos debido á acción combinada da adenilato quinase e os controis da fosforilación oxidativa.
Ata agora identificáronse nove isoformas da proteína ADK humana. Mentres que algunhas están presentes na maioría dos tecidos do corpo, algunhas están localizadas só en tecidos ou partes da célula específicos. Por exemplo, a ADK7 e a ADK8 só se encontran no citosol das células; e a ADK7 encóntrase no músculo esquelético, mentres que ADK8 non.[3] Non só varía a localización das isoformas dentro da célula, senón que a unión ao substrato do encima e a cinética da transferencia do fosforilo son tamén diferentes. A ADK1, é a isocima ADK máis abundante no citosol, ten unha Km unhas mil veces máis alta que as Km de ADK7 e 8, indicando unha unión moito máis feble da ADK1 co AMP.[4] A localización subcelular dos encimas ADK faise incluíndo unha secuencia diana na proteína.[3] Cada isoforma tamén ten unha diferente preferencia polos nucleósidos trifosfato (NTPs). Algúns só usan o ATP, mentres que outros aceptan GTP, UTP e CTP como portadores do fosforilo.
Algunhas destas isoformas prefiren outros NTPs. Hai unha GTP:AMP fosfotransferase mitocondrial, tamén específica para a fosforilación de AMP, que só pode usar GTP ou ITP como doante de fosforilos.[5] A ADK foi tamén identificada en diferents especies de bacterias e en lévedos.[6] Coñécense outros dous encimas máis relacionados coa familia da ADK, que son a uridín monofosfoquinase de lévedos e a UMP-CMP quinase de mofos mucilaxinosos. Algúns residuos están conservados nas distintas isoformas, o que indica o esenciais que son para a catálise. Unha das áreas máis conservadas inclúe un residuo Arg, cuxa modificación inactiva o encima, xunto cun Asp que se sitúa na fenda catalítica do encima e participa nunha ponte salina.
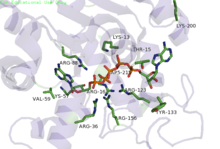
A transferencia de fosforilos só ocorre cambiando á conformación Pechada o dominio 'LID Aberto' do encima. Isto causa unha exclusión de moléculas de auga que deixa os substratos próximos uns a outros,[7] diminuíndo a barreira de enerxía para o ataque nucleofílico polo α-fosforilo do AMP sobre o grupo γ-fosforilo do ATP, que orixina a formación de ADP por transferencia do grupo γ-fosforilo ao AMP. Na estrutura cristalina do encima ADK de Escherichia coli co inhibidor Ap5A, o residuo Arg88 únese ao Ap5A no grupo α-fosfato. Observouse que a mutación R88G causa unha perda do 99% da actividade catalítica deste encima, o que suxire que este residuo está estreitamente implicado na transferencia de fosforilos.[8] Outro residuo moi conservado é a Arg119, que está na rexión de unión da adenosina na ADK, e actúa facendo de sándwich coa adenina no sitio activo. Suxeriuse que a promiscuidade destes encimas ao aceptaren outros NTPs débese ás interaccións relativamente sen importancia da base no peto de unión do ATP.[9] Unha rede positiva de residuos conservados (Lys13, Arg123, Arg156 e Arg167 na ADK de E. coli) estabiliza a acumulación de cargas negativas sobre o grupo fosforilo durante a transferencia. Dous residuos de aspartato distais únense á rede de arxininas, causando que o encima sufra un pregamento e reduza a súa flexibilidade. Tamén é necesario o [[magnesio] como cofactor, esencial para incrementar a electrofilicidade do fosfato sobre o AMP, aínda que este ión magnesio só se mantén no peto activo por interaccións electrostáticas e disóciase doadamente.[9]

A flexibilidade e plasticidade permite que as proteínas se unan a ligandos, formen oligómeros, se agreguen e realicen traballos mecánicos.[10] Grandes cambios conformacionais nas proteínas desempeñan un importante papel na sinalización celular. A adenilato quinase é unha proteína de transdución de sinais; así, o balance entre as conformacións regula a actividade da proteína.[11]

Un estudo de 2007 feito por Whitford et al. mostra as conformacións da ADK cando se une ao ATP ou AMP.[10] O estudo mostra que hai tres conformacións ou estruturas relevantes da ADK: CORE, Aberta e Pechada. Na ADK, hai dous pequenos dominios chamados o LID e o NMP.[12] O ATP únese no peto formado polos dominios LID e CORE. O AMP únese ao peto formado polo dominios NMP e CORE. O estudo de Whitford tamén descubriu que rexións localizadas da proteína despregábanse durante as transicións conformacionais. Este mecanismo reduce a tensión e mellora a eficiencia catalítica. O despregamento local é o resultado das enerxías de tensión en competencia na proteína.[10]
A estabilidade termodinámica local dos dominios de unión ao substrato ATPlid e AMPlid é significativamente menor cando se compara co dominio CORE da ADKE. coli.[13] Ademais, os dous subdominios (ATPlid e AMPlid) poden pregarse de "maneira non cooperativa".[13] A unión dos susbstratos causa unha preferencia polas conformacións 'pechadas' entre todas as que mostrea a ADK (nas paisaxes de enerxía). Estas conformacións 'pechadas' hipotetízase que axudan a retirar a auga do sitio activo para evitar hidrólises inútiles de ATP ademais de contribuíren a optimizar o aliñamento dos substratos para a transferencia de fosforilos.[14] Ademais, o apoencima aínda mostrea as conformacións 'pechadas' dos dominios ATPlid e AMPlid en ausencia de substratos.[7] Cando se compara a taxa de apertura do encima (que permite a liberación do produto) e a taxa de peche que acompaña a unión do substrato, a apertura é o proceso máis lento.
A capacidade dunha célula de medir termodinamicamente os niveis enerxéticos proporciónalle un método para monitorizar os procesos metabólicos.[15] Ao monitorizar continuamente e alterar os niveis de ATP e os outros adenil fosfatos (niveis de ADP e AMP), a adenilato quinase é un importante regulador do gasto de enerxía a nivel celular.[16] A medida que cambian os niveis de enerxía baixo deiferentes estreses metabólicos a adenilato quinase pode entón xerar AMP, e este composto actúa como unha molécula de sinalización nas seguintes fervenzas de sinalización. Este AMP xerado pode, por exemplo, estimular varios receptores dependentes de AMP como os que interveñen nas vías glicolíticas, canles de K-ATP, e proteína quinase activada por AMP (AMPK).[15] Factores comúns que inflúen nos niveis de nucleótidos de adenina, e, por tanto, na actividade da ADK, son o exercicio, o estrés, cambios nos niveis de hormonas e a dieta.[15] Isto facilita a descodficación da información celular ao catalizar intercambios de nucleótidos na íntima “zona detectora” dos sensores metabólicos.[15]
A adenilato quinase está presente nos compartimentos mitocondrial e miofibrilar da célula, e proporciona dous fosforilos de alta enerxía (β e γ) do ATP para que sexan transferidos entre moléculas de nucleótidos de adenina.[15][16] En esencia, a adenilato quinase transporta ATP a sitios de alto consumo de enerxía e retira o AMP xerado no decurso destas reaccións. Estas fosfotransferencias secuenciais teñen en último extremo como resultado a propagación de grupos fosforilos entre conxuntos de moléculas de ADK.[15] Este proceso pode entenderse como unha "cadea humana" (neste caso de moléculas) de ADK que produce cambios no fluxo metabólico local sen cambios aparentes globais nas concentracións de metabolitos.[15] Este proceso é extremadamente importante para a homeostase global da célula.[15]
A nucleósido difosfato quinase é un encima que cataliza in vivo a síntese dependente de ATP de ribo- e desoxirribonucleósidos trifosfato. En bacterias mutadas de Escherichia coli que tiñan unha nucleósido difosfato quinase alterada, a adenilato quinase realizaba unha función encimática dobre, xa que complementaba a deficiencia en nucleósido difosfato quinase.[17]
A deficiencia en adenilato quinase no eritrocito está asociada coa anemia hemolítica.[18] Esta é unha rara eritroencimopatía hereditaria que nalgúns casos está asociada con atraso mental e discapcidade psicomotora.[19] Informouse de polo menos dous pacientes que experimentaron ictericia neonatal e esplenomegalia e requiriron transfusións de sangue debido a esta deficiencia.[20] Noutro paciente un fragmento anormal con substitucións A → G homocigotas e heterocigotas no codón 164 causaron graves deficiencias na ADK de eritrocitos.[21] Estudouse tamén o caso de dous irmáns que tiñan deficiencia na ADK do eritrocito, pero un non presentou evidencias de hemólise.[22]
O knockout de AK1 altera a sincronía entre o fosfato inorgánico e o recambio dos sitios que gastan ATP e os que o sintetizan. Isto reduce a comunicación do sinal enerxético no corazón postísquémico e precipita o refluxo coronario inadecuado despois de isquemia e reperfusión.[23]
A deficiencia en adenilato quinase 2 (AK2) en humanos causa defectos hematopoéticos asociados con perda de audición.[24] A disxénese reticular é unha forma autosómica recesiva de inmunodeficiencia combinada humana. Tamén se caracteriza por unha alteración da maduración linfoide e unha detención temperá da diferenciación na liñaxe linfoide. A deficiencia en AK2 ten como resultado a ausencia ou unha gran diminución na expresión de proteínas. A AK2 exprésase especificamente na estría vascular do oído interno, o que indica por que as persoas con deficiencia de AK2 teñen perda de audición.[24]
A ablación xenética de AK1 diminúe a tolerancia ao estrés metabólico. A deficiencia de AK1 induce unha variación específica de tipo de fibra muscular en grupos de transcritos na glicólise e o metabolismo mitocondrial e en produtos xénicos que definen eventos estruturais e mioxénicos.[25] Isto apoia o metabolismo enerxético muscular.
Na planta Arabidopsis thaliana observouse un maior cerecemento e unha elevación na biosíntese de aminoácidos durante a fotosíntese asociados coa dificiencia de adenilato quinase plastidial.[26]
Este artigo incorpora textos en dominio público procedentes de Pfam e InterPro IPR000850